Bài tập tiên đề Bo, tiên đề về các trạng thái dừng, quỹ đạo dừng, bán kính dừng vật lí 12 Lượng tử ánh sáng
Tiên đề Bo về các trạng thái dừng
- Nguyên tử chỉ tồn tại trong một số trạng thái có năng lượng xác định, gọi là các trạng thái dừng. Khi ở trong trạng thái dừng các nguyên tử không bức xạ.
- Trong các trạng thái dừng của nguyên tử, electron chỉ chuyển động xung quanh hạt nhân trên các quĩ đạo có bán kính hoàn toàn xác định gọi là các quỹ đạo dừng.
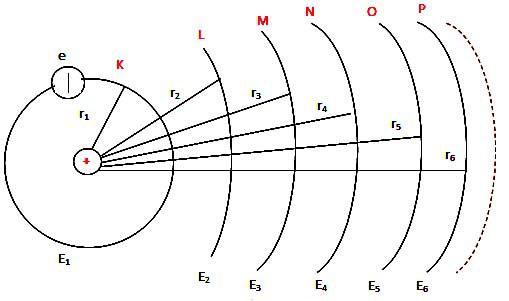
Theo tiên đề Bo về các trạng thái dừng e chuyển động xung quanh hạt nhân ở các quỹ đạo có bán kính xác định các quỹ đạo này sẽ cách hạt nhân một khoảng là r = n2ro
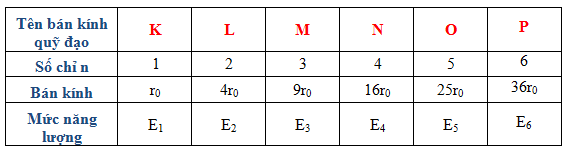
Video hướng dẫn giải bài tập tiên đề BO về trạng thái dừng
Bài tập tiên đề Bo: tiên đề về các trạng thái dừng
Câu 1.
Theo mẫu nguyên tử Bo, trạng thái dừng của nguyên tử
[A]. có thể là trạng thái cơ bản hoặc trạng thái kích thích.
[B]. là trạng thái mà các êlectron trong nguyên tử ngừng chuyển động.
[C]. chỉ là trạng thái kích thích.
[D]. chỉ là trạng thái cơ bản.
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Theo mẫu nguyên tử Bo, trạng thái dừng của nguyên tử có thể là trạng thái cơ bản hoặc trạng thái kích thích
Câu 2.
Theo lí thuyết của Bo về nguyên tử thì
[A]. khi ở các trạng thái dừng, động năng của electron trong nguyên tử bằng 0.
[B]. khi ở trạng thái cơ bản, nguyên tử có năng lượng cao nhất.
[C]. nguyên tử bức xạ chỉ khi chuyển từ trạng thái cơ bản lên trạng thái kích thích.
[D]. trạng thái kích thích có năng lượng càng cao ứng với bán kính quỹ đạo của electron càng lớn.
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Theo lí thuyết của Bo về nguyên tử thì trạng thái kích thích có năng lượng càng cao ứng với bán kính quỹ đạo của electron càng lớn.
Câu 3.
Trong nguyên tử hiđrô , bán kính Bo là \[{{r}_{0}}=5,{{3. 10}^{-11}}m\]. Bán kính quỹ đạo dừng N là
[A]. \[47,{{7. 10}^{-11}}m. \]
[B]. \[21,{{2. 10}^{-11}}m. \]
[C]. \[84,{{8. 10}^{-11}}m. \]
[D]. \[132,{{5. 10}^{-11}}m. \]
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Bán kính quỹ đạo dừng N là \[16{{r}_{0}}=84,{{8. 10}^{-11}}m. \]
Câu 4.
Theo mẫu nguyên tử Bo, bán kính quỹ đạo dừng N của êlectron trong nguyên tử hiđrô là
[A]. \[47,{{7. 10}^{11}}m. \]
[B]. \[132,{{5. 10}^{11}}m. \]
[C]. \[21,{{2. 10}^{11}}m. \]
[D]. \[84,{{8. 10}^{11}}m. \]
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Bán kính quỹ đạo dừng N là \[16{{r}_{0}}=84,{{8. 10}^{-11}}m. \]
Câu 5.
Theo mẫu nguyên tử Bo, một nguyên tử hiđrô đang ở trạng thái cơ bản, êlectron chuyển động trên quỹ đạo dừng có bán kính \[{{r}_{0}}\]. Khi nguyên tử này hấp thụ một phôtôn có năng thì êlectron có thể chuyển lên quỹ đạo dừng có bán kính bằng
[A]. \[11{{r}_{0}}. \]
[B]. \[10{{r}_{0}}. \]
[C]. \[12{{r}_{0}}. \]
[D]. \[9{{r}_{0}}. \]
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Nó chỉ chuyển lên quỹ đạo có bán kính xác định dạng : \[{{n}^{2}}{{r}_{0}}\Rightarrow \] chỉ có D thỏa mãn khi n = 3
Câu 6.
Gọi \[{{r}_{0}}\] là bán kính quỹ đạo dừng thứ 1 nhất của nguyên tử hiđro. Khi bị kích thích nguyên tử hiđro không thể có quỹ đạo:
[A]. \[2{{r}_{0}}\]
[B]. \[4{{r}_{0}}\]
[C]. \[16{{r}_{0}}\]
[D]. \[9{{r}_{0}}\]
Nó chỉ chuyển lên quỹ đạo có bán kính xác định dạng : \[{{n}^{2}}{{r}_{0}}\Rightarrow \] chỉ có A không thỏa mãn
Câu 7.
Theo mẫu nguyên tử Bo, bán kính quỹ đạo K của êlectron trong nguyên tử hiđrô là \[{{r}_{0}}\]. Khi êlectron chuyển từ quỹ đạo N về quỹ đạo L thì bán kính quỹ đạo giảm bớt
[A]. \[12{{r}_{0}}. \]
[B]. \[4{{r}_{0}}. \]
[C]. \[9{{r}_{0}}. \]
[D]. \[16{{r}_{0}}\] .
Ở N thì quỹ đạo là \[16{{r}_{0}}\] và ở L thì quỹ đạo là \[4{{r}_{0}}\], vậy khi chuyển từ N về L thì nó giảm \[12{{r}_{0}}\]
Câu 8.
Theo mẫu nguyên tử Borh, bán kính quĩ đạo K của electron trong nguyên tử hidro là \[{{r}_{0}}\]. Khi electron chuyển từ quĩ đạo M về quĩ đạo O thì bán kính quĩ đạo sẽ
[A]. tăng\[12{{r}_{0}}\]
[B]. tăng \[9{{r}_{0}}\]
[C]. giảm \[9{{r}_{0}}\]
[D]. tăng \[16{{r}_{0}}\]
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Ở M thì quỹ đạo là \[9{{r}_{0}}\] và ở O thì quỹ đạo là \[25{{r}_{0}}\] , vậy khi chuyển từ M lên L thì nó tăng \[16{{r}_{0}}\]
Câu 9.
Trong nguyên tử hiđrô, bán kính Bo là \[{{r}_{0}}=5,{{3. 10}^{-11}}m\]. Ở một trạng thái kích thích của nguyên tử hiđrô, êlectron chuyển động trên quỹ đạo dừng có bán kính là \[r=2,{{12. 10}^{-10}}m\]. Quỹ đạo đó có tên gọi là quỹ đạo dừng
[A]. L.
[B]. O.
[C]. N.
[D]. M.
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Nhận thấy \[r=4{{r}_{0}}\Rightarrow \] Ở quỹ đạo L
Câu 10.
Biết bán kính Bo là \[{{r}_{0}}=5,{{3. 10}^{-11}}m\]. Bán kính quỹ đạo dừng M trong nguyên tử hidro là:
[A]. \[132,{{5. 10}^{-11}}m\]
[B]. \[84,{{8. 10}^{-11}}m\]
[C]. \[21,{{2. 10}^{-11}}m\]
[D]. \[47,{{7. 10}^{-11}}m. \]
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Bán kính quỹ đạo M là \[9{{r}_{0}}=47,{{7. 10}^{-11}}m\]
Câu 11.
Trong nguyên tử hiđrô, bán kính quỹ đạo dừng M của eletron là 4,77 $\overset{o}{\mathop{A}}\,$, quỹ đạo dừng của electron có bán kính 19,08 $\overset{o}{\mathop{A}}\,$ có tên gọi là
[A]. L.
[B]. O.
[C]. N.
[D]. P.
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Ta thấy : \[19,08=4. 4,77\Rightarrow \] Quỹ đạo cần tìm là quỹ đạo L
Câu 12.
Theo mẫu nguyên tử Bo, trong nguyên tử hiđrô, chuyển động của êlectron quanh hạt nhân là chuyển động tròn đều. Gọi v là tốc độ của electron trên quỹ đạo K. Khi nhảy lên quỹ đạo N, electron có tốc độ bằng
[A]. $\dfrac{v}{9}$.
[B]. 4v.
[C]. $\dfrac{v}{2}$.
[D]. $\dfrac{v}{4}$.
Theo định luật Culông, lực tương tác giữa e và hạt nhân nguyên tử H có độ lớn là: $F=k\dfrac{{{e}^{2}}}{{{r}^{2}}}$ Lực Culông đóng vai trò lực hướng tâm nên: $F=k\dfrac{{{e}^{2}}}{{{r}^{2}}}=\dfrac{m{{v}^{2}}}{r}\Rightarrow v=e\sqrt{\dfrac{k}{m\text{r}}}=4,4. \text{ }{{10}^{5}}m/s. $ \[\dfrac{{{v}_{N}}}{{{v}_{K}}}=\sqrt{\dfrac{{{\text{r}}_{K}}}{{{\text{r}}_{N}}}}=\sqrt{\dfrac{1}{16}}\Rightarrow {{v}_{N}}=\dfrac{{{v}_{K}}}{4}\]
Câu 13.
Theo mẫu nguyên tử Bo, trong nguyên tử hiđrô, chuyển động của êlectron quanh hạt nhân là chuyển động tròn đều. Trong nguyên tử hidro bán kính quỹ đạo K là \[{{r}_{0}}=5,{{3. 10}^{-11}}m\]. cho hằng số điện $k={{9. 10}^{9}}\dfrac{N{{m}^{2}}}{{{C}^{2}}}$;\[{{m}_{e}}=9,{{1. 10}^{-31}}kg,e=1,{{6. 10}^{-19}}C\] . Hãy tính bán kính quỹ đạo O và tốc độ electron trên quỹ đạo đó.
[A]. \[r=2,65{{A}^{0}};v=4,{{4. 10}^{5}}m/s. \]
[B]. \[r=13,25{{A}^{0}};v=1,{{9. 10}^{5}}m/s. \]
[C]. \[r=13,25{{A}^{0}};v=4,{{4. 10}^{5}}m/s. \]
[D]. \[r=13,25{{A}^{0}};v=3,{{09. 10}^{5}}m/s. \]
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Theo định luật Culông, lực tương tác giữa e và hạt nhân nguyên tử H có độ lớn là: $F=k\dfrac{{{e}^{2}}}{{{r}^{2}}}$ Lực Culông đóng vai trò lực hướng tâm nên: $F=k\dfrac{{{e}^{2}}}{{{r}^{2}}}=\dfrac{m{{v}^{2}}}{r}\Rightarrow v=e\sqrt{\dfrac{k}{m\text{r}}}=4,4. \text{ }{{10}^{5}}m/s. $
Câu 14.
Electron trong nguyên tử hydro quay quanh hạt nhân trên các quỹ đạo tròn gọi là quỹ đạo dừng. Biết tốc độ của electron trên quỹ đạo K là \[2,{{186. 10}^{6}}m/s\]. Khi electron chuyển động trên quỹ dừng N thì vận tốc của nó là
[A]. \[2,{{732. 10}^{5}}m/s\]
[B]. \[5,{{465. 10}^{5}}m/s\]
[C]. \[8,{{198. 10}^{5}}m/s\]
[D]. \[10,{{928. 10}^{5}}m/s\]
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Theo định luật Culông, lực tương tác giữa e và hạt nhân nguyên tử H có độ lớn là: $F=k\dfrac{{{e}^{2}}}{{{r}^{2}}}$ Lực Culông đóng vai trò lực hướng tâm nên: $F=k\dfrac{{{e}^{2}}}{{{r}^{2}}}=\dfrac{m{{v}^{2}}}{r}\Rightarrow v=e\sqrt{\dfrac{k}{m\text{r}}}$ \[\dfrac{{{v}_{N}}}{{{v}_{K}}}=\sqrt{\dfrac{{{\text{r}}_{K}}}{{{\text{r}}_{N}}}}=\sqrt{\dfrac{1}{16}}\Rightarrow {{v}_{N}}=\dfrac{{{v}_{K}}}{4}=5,465. \text{ }{{10}^{5}}m/s. \]
Câu 15.
Theo thuyết Bo ,bán kính quỹ đạo thứ nhất của electron trong nguyên tử hidro là\[{{r}_{0}}=5,{{3. 10}^{-11}}m\] , cho hằng số điện $k={{9. 10}^{9}}\dfrac{N{{m}^{2}}}{{{C}^{2}}}$,\[e=1,{{6. 10}^{-19}}C,{{m}_{e}}=9,{{1. 10}^{-31}}kg\]. Hãy xác định vận tốc góc của electron chuyển động tròn đều quanh hạt nhân trên quỹ đạo thứ nhất này.
[A]. \[6,{{8. 10}^{16}}rad/s\]
[B]. \[2,{{4. 10}^{16}}rad/s\]
[C]. \[4,{{6. 10}^{16}}rad/s\]
[D]. \[4,{{1. 10}^{16}}rad/s\]
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Tốc góc của electron chuyển động tròn đều quanh hạt nhân trên quỹ đạo thứ nhất này là : $\omega =\dfrac{v}{r}$= $\sqrt{\dfrac{k{{e}^{2}}}{m{{r}^{3}}}}$= \[4,{{1. 10}^{16}}rad/s\]
Câu 16.
Theo mẫu nguyên tử Bo, trong nguyên tử hiđrô, chuyển động của êlectron quanh hạt nhân là chuyển động tròn đều. Tỉ số giữa tốc độ của êlectron trên quỹ đạo K và tốc độ của êlectron trên quỹ đạo M bằng
[A]. 9.
[B]. 2.
[C]. 3.
[D]. 4.
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Ta có $v=\sqrt{\dfrac{k{{e}^{2}}}{mr}}$$\Rightarrow $$v\sim \dfrac{1}{\sqrt{r}}$( tỉ lệ ) $\Rightarrow $ đáp án cần tìm là C: 3
Câu 17.
Êlectron trong nguyên tử Hidrô chuyển từ quỹ đạo dừng có mức năng lượng lớn về quỹ đạo dừng có mức năng lượng nhỏ hơn thì vận tốc êlectron tăng lên 2,5 lần. Êlectron có thể đã chuyển từ quỹ đạo
[A]. O về L.
[B]. O về K.
[C]. N về K.
[D]. N về L.
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Theo Mẫu nguyên tử Bo, lực Cu-lông đóng vai trò là lực hướng tâm gây ra chuyển động của electron: $k\dfrac{{{e}^{2}}}{{{r}^{2}}}={{m}_{e}}\dfrac{v_{n}^{2}}{r}\Rightarrow {{v}_{n}}=\sqrt{k\dfrac{{{e}^{2}}}{{{m}_{e}}. {{r}^{{}}}}}$ + Khi electron ở quỹ đạo có mức năng lượng lớn: ${{v}_{1}}=\sqrt{k\dfrac{{{e}^{2}}}{{{m}_{e}}. {{r}_{1}}^{{}}}}$ + Khi electron chuyển về quỹ đạo có mức năng lượng nhỏ: ${{v}_{2}}=\sqrt{k\dfrac{{{e}^{2}}}{{{m}_{e}}. {{r}_{2}}^{{}}}}$ + Lập tỉ số: \[\dfrac{{{v}_{1}}}{{{v}_{2}}}=\sqrt{\dfrac{{{r}_{2}}}{{{r}_{1}}}}=2,5\Rightarrow \dfrac{{{r}_{2}}}{{{r}_{1}}}=6,25\Rightarrow {{r}_{2}}=\dfrac{25}{4}{{r}_{1}}\] $\Rightarrow $ Nó có thể được chuyển từ O về L.
Câu 18.
Theo mẫu Bo về nguyên tử hiđrô, nếu lực tương tác tĩnh điện giữa êlectron và hạt nhân khi êlectron chuyển động trên quỹ đạo dừng L là F thì khi electron chuyển động trên quỹ đạo dừng N, lực này sẽ là
[A]. F/16.
[B]. F/25.
[C]. F/9.
[D]. F/4.
Hướng dẫn giải Bài tập tiên đề Bo: trạng thái dừng
Quỹ đạo L có\[n=2\Rightarrow {{r}_{L}}={{n}^{2}}{{r}_{0}}=4{{r}_{0}}\] ; Quỹ đạo N có \[n=4\Rightarrow {{r}_{N}}={{n}^{2}}{{r}_{0}}=16{{r}_{0}}. \] $F=\dfrac{k|qq|}{{{r}^{2}}}\Rightarrow \dfrac{{{F}_{L}}}{{{F}_{N}}}=\dfrac{r_{N}^{2}}{r_{L}^{2}}=16$.
Câu 19.
Theo thuyết Bo, electron trong nguyên tử hidro chuyển động tròn đều trên các quỹ đạo dừng có bán kính ${{r}_{n}}={{n}^{2}}{{r}_{o}}$(\[{{r}_{0}}=5,{{3. 10}^{-11}}m\]), cho hằng số điện $k={{9. 10}^{9}}\dfrac{N{{m}^{2}}}{{{C}^{2}}}$;\[{{m}_{e}}=9,{{1. 10}^{-31}}kg,e=1,{{6. 10}^{-19}}C\]. Tốc độ của e trên quỹ đạo dừng thứ hai:
[A]. \[2,{{18. 10}^{6}}m/s\]
[B]. \[2,{{18. 10}^{5}}m/s\]
[C]. \[1,{{09. 10}^{6}}m/s\]
[D]. \[1,{{98. 10}^{6}}rad/s\]
Ta có $v=\sqrt{\dfrac{k{{e}^{2}}}{mr}}$= \[1,{{09. 10}^{6}}m/s\]
Câu 20.
Electron trong nguyên tử hyđro chuyển từ quỹ đạo dừng có mức năng lượng lớn về quỹ đạo dừng có mức năng lượng nhỏ hơn thì tốc độ electron tăng lên 4 lần. Electron có thể đã chuyển từ quỹ đạo
[A]. N về M.
[B]. M về L.
[C]. N về K.
[D]. N về L.
Bài tập tiên đề Bo: trạng thái dừng, vật lí 12
Theo Mẫu nguyên tử Bo, lực Cu-lông đóng vai trò là lực hướng tâm gây ra chuyển động của electron: $k\dfrac{{{e}^{2}}}{{{r}^{2}}}={{m}_{e}}\dfrac{v_{n}^{2}}{r}\Rightarrow {{v}_{n}}=\sqrt{k\dfrac{{{e}^{2}}}{{{r}^{{}}}}}$ + Khi electron ở quỹ đạo có mức năng lượng lớn: ${{v}_{1}}=\sqrt{k\dfrac{{{e}^{2}}}{{{r}_{1}}^{{}}}}$ + Khi electron chuyển về quỹ đạo có mức năng lượng nhỏ: ${{v}_{2}}=\sqrt{k\dfrac{{{e}^{2}}}{{{r}_{2}}^{{}}}}$ + Lập tỉ số: \[\dfrac{{{v}_{1}}}{{{v}_{2}}}=\sqrt{\dfrac{{{r}_{2}}}{{{r}_{1}}}}=4\Rightarrow \dfrac{{{r}_{2}}}{{{r}_{1}}}=16\Rightarrow {{r}_{2}}=16{{r}_{1}}\] $\Rightarrow $ Nó có thể là chuyển từ N về K
Câu 21.
Theo mẫu nguyên tử Bo, trong nguyên tử hiđrô, chuyển động của êlectrôn quanh hạt nhân là chuyển động tròn đều. Biết hằng số điện $k={{9. 10}^{9}}\dfrac{N{{m}^{2}}}{{{C}^{2}}}$;\[e=1,{{6. 10}^{-19}}C;{{m}_{e}}=9,{{1. 10}^{-31}}kg\] . Tốc độ của êlectrôn khi nó chuyển động trên quỹ đạo có bán kính \[{{r}_{0}}=5,{{3. 10}^{-11}}m\] (quỹ đạo K) và tần số chuyển động tròn đều của êlectrôn là
[A]. \[v=2,{{2. 10}^{6}}m/s;f=6,{{6. 10}^{15}}v\grave{o}ng/gi\hat{a}y\]
[B]. \[v=2,{{2. 10}^{4}}m/s;f=6,{{6. 10}^{18}}v\grave{o}ng/gi\hat{a}y\]
[C]. \[v=2,{{2. 10}^{6}}km/s;f=6,{{6. 10}^{15}}v\grave{o}ng/gi\hat{a}y\]
[D]. Các giá trị khác.
Bài tập tiên đề Bo: trạng thái dừng, vật lí 12
– Tốc độ của êlectrôn khi nó chuyển động trên quỹ đạo có bán kính \[{{r}_{0}}=5,{{3. 10}^{-11}}m\] (quỹ đạo K) là : $v=\sqrt{\dfrac{k{{e}^{2}}}{mr}}$=\[2,{{2. 10}^{6}}m/s\] – Tần số chuyển động tròn đều của êlectrôn là : ; $f=\dfrac{\omega }{2\pi }=\dfrac{v}{2\pi r}$= \[f=6,{{6. 10}^{15}}v\grave{o}ng/gi\hat{a}y\]